🙋什麼是腎上腺亢進?
👩⚕️腎上腺亢進也稱為庫興氏症(Cushing’s syndrome) 是因為內源性的類固醇(身體自己產生的類固醇)或是外源性類固醇(給予過多外用的類固醇)過多,而出現頻渴,多尿與食慾過度旺盛等症狀。
➡️可分成 促腎上腺皮質素相關性 (ACTH -adrenocorticotropic hormone dependent ) ,
佔病例中的85% 。此種大多數與腦下垂體中的良性腫瘤相關:PDH (pituitary dependent hypercortisolism )。另一種是與促腎上腺皮質素無關(ACTH independent), 此種則與腎上腺的腫瘤( adrenal - dependent hypercortisolism ) 相關
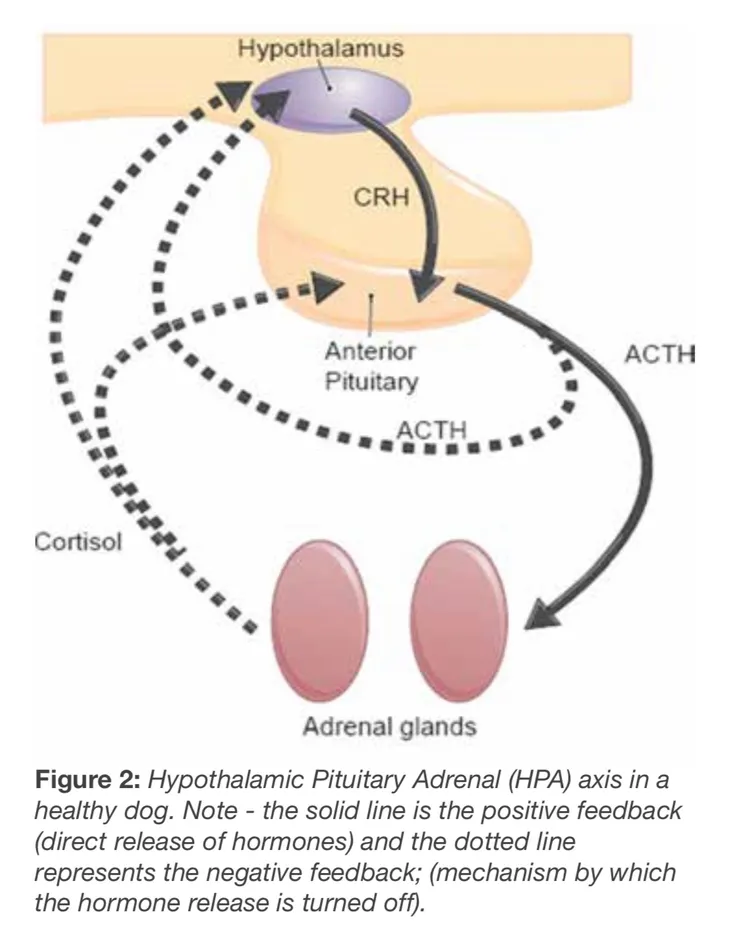
下視丘 腦垂腺(腦下垂體)腎上腺軸
➡️腎上腺的位置在左右腎臟的前內側,是上在上方的一個內分泌腺體(如下圖)
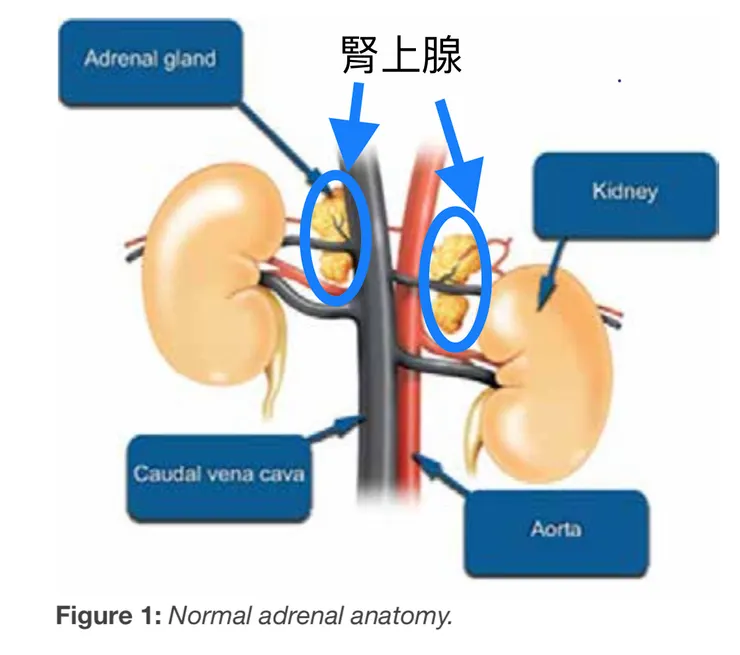
腎上腺的解剖位置
🙋腎上腺亢進的盛行率高嗎?
👩⚕️有一個研究指出在一般私人診所的盛行率約為0.2% , 但在教學醫院則為1.46%。
平均得病年齡為9.8歲。母犬有比公犬有更高的得病機率。
標準雪納瑞,查理士王子獵犬,西施,貴賓犬,臘腸犬,傑克羅素梗,比特犬,拳師犬,馬爾濟斯,約克夏等是好發犬種。
🙋什麼樣的病患需要測試是否有腎上腺亢進呢?
👩⚕️一般是建議在有“臨床症狀“的動物才建議檢測!所謂的臨床症狀包含,腹圍膨大,喘,肌肉萎縮,肌肉僵直(cushing‘s myotonia, pseudomyotonia),皮膚變薄,食慾增加,多渴多尿等等。因為這是一個慢性疾病,通常會發展數個月到數年,所以會有一些症狀慢慢出現,飼主才會帶來看醫生。
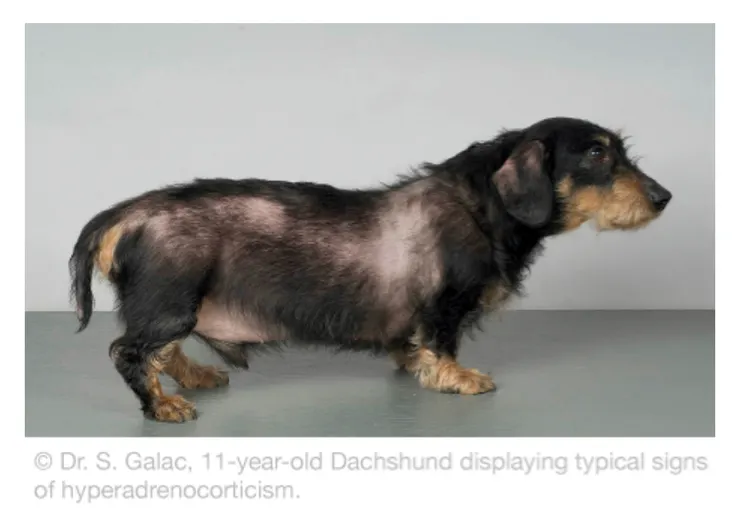
腎上腺亢進病患
➡️但如果只有血檢上看到某個血檢指數偏高,如ALKP(serum alkaline phosphate) 但這隻動物看起來很健康,那麼就算做了檢驗,也會很難判定檢驗結果是否有意義!因為檢測很容易出現偽陽性或是偽陰性。
➡️如果動物正在生病 (例如有其他食慾減退嘔吐或是體重下降等症狀)建議不要測試腎上腺亢進。因為其他疾病可能會干擾內分泌疾病的測試。而且診斷腎上腺亢進也不是一個需要緊急測試的檢查!
不過最終判斷還是要依據您的獸醫師的臨床判斷喔!
🙋有腎上腺亢進的動物會出現什麼併發症呢?
👩⚕️
➡️高血壓:
📍在腎上腺亢進的狗,會有31-86%的機率有高血壓。高血壓改善跟腎上腺亢進本身疾病控制的良好與否沒有明顯相關,所以除了給予腎上腺亢進的藥物,通常還是需要用血壓藥物治療,一般建議先用血管張力素轉化酶抑制劑 (ACEI )血管緊張素受體拮抗劑(ARB) 再來才是用鈣離子通道阻斷劑(calcium chanel blocker)。
📍雖然在人的腎上腺亢進,高血壓與高死亡率相關,但在狗血壓的高低與生存時間沒有明顯相關,但因為血壓仍會造成一些後續影響,所以仍非常建議腎上腺亢進病患需要定期監控血壓。
➡️糖尿病:
📍在一個研究中235隻患有腎上腺亢進的狗中有13.6%的狗出現糖尿病的狀況,空腹血糖如果>105mg/dL 且出現高血脂症(包含三酸甘油脂超過221mg/dL 且膽固醇超過351mg/dL) UCCR > 100 ×10 -6 會有比較高機率演變成糖尿病。
📍而同時患有糖尿病的腎上腺亢進患者生存期會比單純只有糖尿病的患者差
📍但跟只單純患有腎上腺亢進患者沒有明顯差異
📍比單純只有糖尿病的狗有需要比較高的胰島素劑量。
📍早期偵測腎上腺亢進患者的狀態,並且控制好腎上腺亢進的疾病狀態,可以減少演變成糖尿病的機率。
➡️因為食慾增加導致體重過重。
➡️反覆的感染: 例如下泌尿道感染,皮膚感染等。
➡️神經症狀的出現:會因為腦下垂體的腫瘤變大壓迫造成。
➡️肺栓塞與血栓的出現
📍 較高的血小板數量與生存時間相關(可能跟高凝血狀態導致較高血栓生成機率相關,但目前沒有研究直接證實高血小板數量與血栓生產之間直接的相關性)。
➡️皮膚變薄,毛皮生長不好,皮膚鈣化等。
📍皮膚鈣化(calcinosis cutis) (441 vs 1103 days) 在這樣的病患中血磷與PTH也會上升,如果使用trilostane 治療PDH的狗血磷大於4.5的狗存活率會比小於4.5mg/dl的狗存活率差。
📍體態評分小於三分body condition score (BCS ≤3/9 ) (261 vs 998 days) (也可能跟比較瘦的狗有比較多的共病症有關)
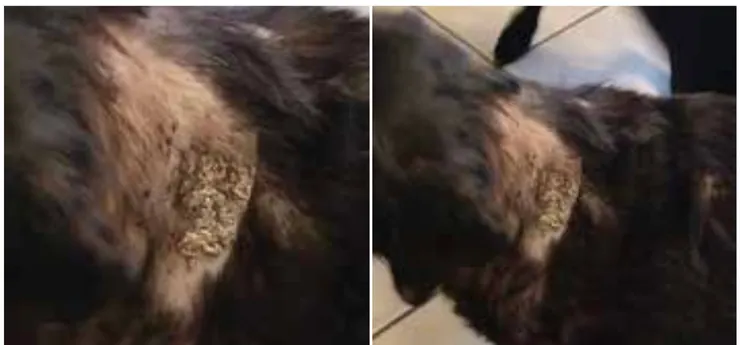
腎上腺亢進造成的皮膚鈣化
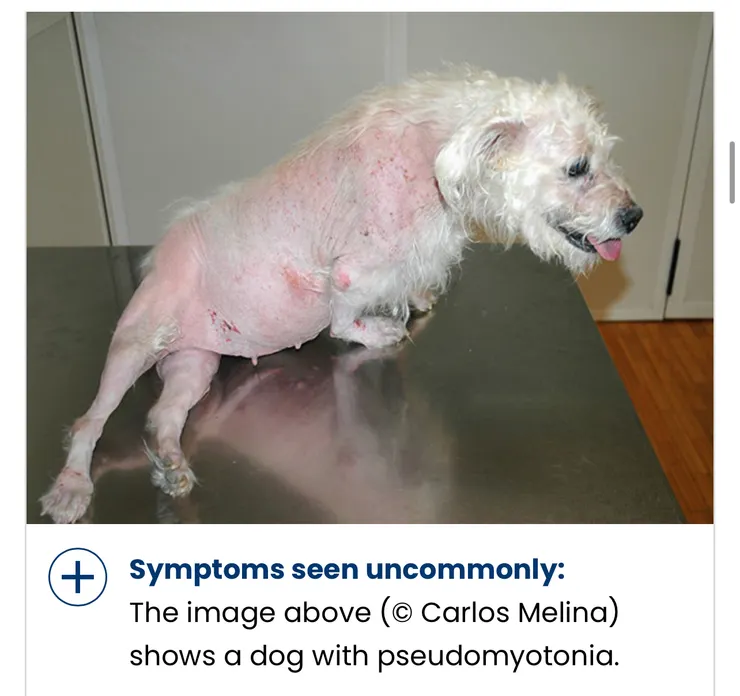
腎上腺亢進造成的肌肉僵直(但腎上腺亢進患者以肌肉無力症狀相較僵直常見)
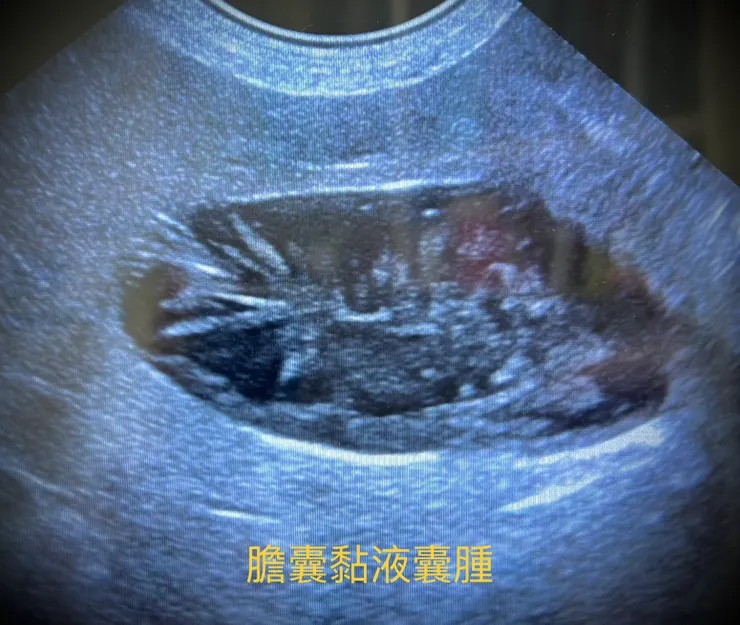
➡️膽囊遲滯疾病如膽囊黏液囊腫。
🙋 如果動物有臨床症狀,那麼我就可以開始測試了嗎?
👩⚕️ 如果有臨床症狀,的確可以開始測試
➡️但很重要的一件事,是要確定這個病患在之前沒有被使用過外源性的類固醇,包含使用外用耳藥,皮膚藥膏,或是含有類固醇的眼藥等。甚至也要跟主人確認飼主本身是否有在擦拭類固醇藥膏,因為有些狗會舔飼主的皮膚,這點也需要注意!
➡️ 在做內分泌測試之前也建議先做基礎的血液檢查包含紅白血球生化指數,尿檢等,也可以從這些臨床病理的參數去輔助診斷內分泌疾病。通常會看到的血液變化包含肝膽指數,血清鹼性磷酸酶ALKP 上升與丙胺酸轉胺 ALT的上升(但幅度通常ALKP上升的幅度小),尿比重偏低( 尿比重低於1.020),血中膽固醇上升,血小板與總紅血球容積(PCV)輕微上升,高血壓,出現蛋白尿等。
➡️如果飼主沒有發現臨床症狀但是只有檢查時出現臨床病理症狀,最常見的就是測試到血檢中的ALKP變高,此時您的獸醫通常會先再仔細詢問是否有些症狀沒有被注意到,但如果真的沒有症狀,可以先做尿液檢測排除疾病。
➡️下表是2023年美國動物醫院協會AAHA整理了各種不同情況上的腎上腺亢進建議診斷指引

References
• Behrend, E.N. et al. (2013) ‘Diagnosis of spontaneous canine hyperadrenocorticism: 2012 ACVIM consensus statement (small animal)’, Journal of Veterinary Internal Medicine, 27(6), pp. 1292–1304. doi:10.1111/jvim.12192.
• Bugbee, A. et al. (2023) ‘2023 Aaha selected endocrinopathies of dogs and cats guidelines’, Journal of the American Animal Hospital Association, 59(3), pp. 113–135. doi:10.5326/jaaha-ms-7368.
• Carotenuto, G. et al. (2019) ‘Cushing’s syndrome—an epidemiological study based on a canine population of 21,281 dogs’, Open Veterinary Journal, 9(1), p. 27. doi:10.4314/ovj.v9i1.5.
• García San José, P. et al. (2022) ‘Survival of dogs with pituitary‐dependent hyperadrenocorticism treated twice daily with low doses of Trilostane’, Veterinary Record, 191(3). doi:10.1002/vetr.1630.
• Miceli, D.D., Pignataro, O.P. and Castillo, V.A. (2017) ‘Concurrent hyperadrenocorticism and diabetes mellitus in dogs’, Research in Veterinary Science, 115, pp. 425–431. doi:10.1016/j.rvsc.2017.07.026.
• Pérez-López, L., Mendoza, P. and Melián, C. (2023) ‘Effects of concurrent canine Cushing’s syndrome and diabetes mellitus on insulin requirements, trilostane dose, and Survival Time’, Research in Veterinary Science, 161, pp. 62–68. doi:10.1016/j.rvsc.2023.06.003.
• Wilson, S. (2017) ‘Diagnosing Hyperadrenocorticism FAQ’, Medical FAQs.



















