※如欲轉載本文,請與北美智權報聯絡
吳碧娥╱北美智權報 編輯部
圖片來源 : shutterstock、達志影像
2025年,對於台灣生技醫療產業而言,無疑是極具歷史意義的分水嶺。隨著《再生醫療法》與《再生醫療製劑條例》(下稱「再生醫療雙法」)的三讀通過,台灣再生醫療產業(Regenerative Medicine)從研發走向臨床應用、從法規模糊走向制度完善的關鍵轉折。這不僅為許多面臨未被滿足醫療需求的病患帶來曙光,更為台灣生技產業開啟了接軌國際、競逐全球兆元商機的嶄新大門。
法規的通過只是起跑槍響。當遊戲規則確立,隨之而來的便是資本、技術與產能的較量。這是一場從生醫實驗室到產品化的「軍備競賽」。在全球供應鏈重組與技術迭代的浪潮下,台灣是否能憑藉半導體代工的成功經驗,在再生醫療委託開發暨製造服務(CDMO)領域再造一座護國神山?
CDMO成兵家必爭之地,規模經濟為競爭關鍵
再生醫療被視為繼小分子藥物、蛋白質藥物之後,人類醫學史上的第三次革命。這類療法利用基因、細胞及其衍生物來修復或替換受損組織,涵蓋了CAR-T細胞治療、基因編輯療法及外泌體療法等次世代技術。
歷經了2022與2023年的低谷,全球再生醫療市場正在強勁復甦。2024 年全球再生醫療市場投資金額達152億美元,較前一年明顯回升,顯示資本市場重拾信心。更重要的是,再生醫療產品已從「概念驗證」進入「商業落地」階段。僅2024年,美國FDA便核准了9項新產品,包括每劑425萬美元創下全球最貴紀錄的治療異染性腦白質退化症基因療法Lenmeldy,以及多款針對血友病與罕見疾病的基因療法。
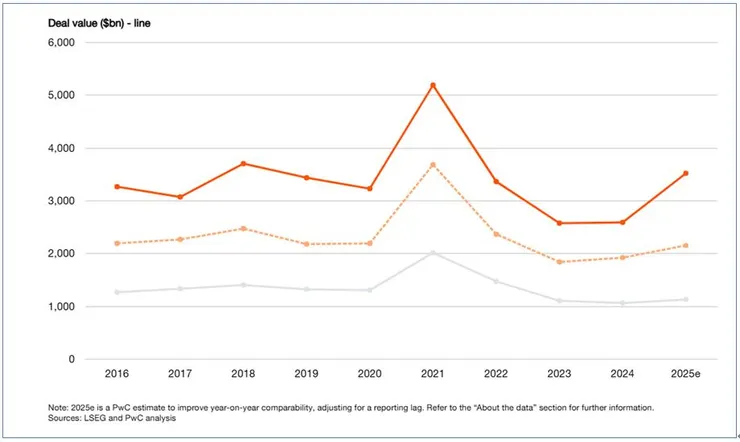
圖1. 2018~2024年再生醫療市場概況;圖片來源:PwC再生醫療與次世代療法產業趨勢報告
然而,這些創新療法的背後,隱藏著巨大的製造挑戰。再生醫療產品多為活細胞或基因載體,具有保存期限短、運送條件嚴苛、製程高度變異且極易受污染的特性。這導致了生產成本居高不下,且良率難以控制。面對高昂的自建廠房成本與複雜的法規門檻,越來越多的研發型生技公司選擇將製造環節外包。全球先進療法CDMO市場因此呈現爆發式成長:2023年市場規模約61億美元,預計將以每年近19%的複合成長率擴張,至2033年達到345.3億美元。CDMO規模與重要性與日俱,已成為再生醫療產業不可或缺的一環。
目前CDMO市場正在經歷類似半導體產業早期的整併。2025年5月,美國投資公司Altaris收購了日本Minaris Regenerative Medicine以及中國藥明康德(WuXi Advanced Therapies)旗下的歐美業務,組建了橫跨三大洲的新巨頭Minaris Advanced Therapies,顯示再生醫療CDMO 產業正朝高度專業化與全球化佈局發展。國際藥廠除了透過擴廠和併購迅速擴大產能與服務範疇;另一方面,市場也出現整合趨勢,打造出跨國跨區域的大型代工平台,規模經濟將成為競爭關鍵。
為了迎接這場全球競賽,隨著雙法上路,台灣已建立起一套與國際接軌、且兼具防禦與攻擊的戰略體系。
「附款許可」:搶攻國際臨床的時間差紅利
《再生醫療製劑條例》中最具戰略價值的條款,莫過於「附款許可」機制。為了平衡加速上市與安全性的需求,針對危及生命或嚴重失能的疾病,若完成二期臨床試驗並證實安全性與初步療效,主管機關可核發附帶條件的臨時許可。
這項制度為新藥開發爭取了寶貴的「時間差」。對於國際藥廠而言,來台進行臨床試驗不僅能獲得高品質的醫療數據,更有機會提前在台上市並產生營收,這將吸引國際大廠將台灣納入多國多中心臨床試驗的一環,台灣擁有優質研發人才與高品質臨床試驗環境,搭配日漸完善的法規體系,有望讓國際藥廠來台設立亞洲區的研發樞紐。
PIC/SGMP:製造門檻升級
過去台灣細胞治療多依循《特管辦法》在醫療機構內小規模執行。新法上路後,製劑的生產必須全面遵循藥物優良製造準則(PIC/SGMP)及西藥優良運銷準則(GDP)。雖然這大幅提高了業者的合規成本與硬體門檻,但也帶動產業升級。目前包括樂迦、台寶、訊聯、國璽等業者皆已佈局臨床級CDMO及自動化製程平台。仲恩生醫則於2024 年獲得日本厚生勞動省(MHLW)核發「再生醫療等製品外國製造業者認定證」,成為台灣首家取得認證的企業,證明台灣的製造品質已具備國際輸出的實力。
AI x ICT:導入AI與機器學習
再生醫療目前最大的痛點在於製造過程複雜而成本高昂、人力密集且難以標準化的操作流程,這正是台灣ICT產業最擅長解決的問題,導入AI與機器學習(AI/ML)可實現非破壞性品管、預測性控制與自動化生產,大幅降低人為誤差與成本。台灣擁有世界級的半導體與精密機械供應鏈,可憑藉半導體與精密製造產業累積的管理經驗,可將自動化技術轉移至高度標準化的生醫製程,以複製高科技產業的成功模式。同時,台灣生技人才基礎紮實,若能爭取國際委託訂單,不僅能培養本土團隊的實戰能量,也可在長期內強化產業競爭力。
台灣面臨兩大結構性挑戰與建議
雖然台灣具備技術與法規優勢,但要成為亞洲再生醫療樞紐,仍面臨兩大結構性挑戰:資金規模不足與產業鏈整合度低。由於再生醫療研發週期長、燒錢速度快,是典型的「高風險、高回報」產業。然而,台灣民間資金相對保守,導致許多新創在早期研發與臨床轉譯階段面臨資金斷鏈。對此,資誠與台灣醫界聯盟基金會建議,政府應強化國發基金的引導角色,推動「超額配比」(Over-Matching)機制,針對具潛力的再生醫療項目,政府提供高於民間創投數倍(如3倍或5倍)的資金配比。這不僅能分攤風險,更能產生訊號效應,帶動民間資本敢於投入高風險但具戰略價值的領域。
組建「CDMO國家隊」
目前台灣的CDMO業者多屬中小型規模,單打獨鬥難以承接國際藥廠的大型訂單。台灣應成立「CDMO策略聯盟」,建立具國際競爭力的CDMO 聚落,整合國內各家業者的產能與技術專長,例如病毒載體、細胞培養、外泌體純化等領域,形成聚合式能量並以「國家隊」的形式對外爭取訂單,並協助廠商提升談判議價能力,強化在全球CDMO供應鏈中的地位。
多元支付與保險創新
再生醫療的天價費用是推動商業化的最大阻礙。單靠全民健保難以支撐動輒數百萬、甚至上億元的新興療法。台灣必須參考日韓經驗,引入商業保險、專案基金或其他創新支付工具,形成健保與民間保險相互分攤的架構,不僅可以減輕健保負擔,更能創造一個有支付能力的內需市場,讓CDMO產業能有穩定的營收來源支持後續研發。
隨著《再生醫療雙法》的完善、PIC/SGMP產線的就位,以及AI智慧製造的導入,台灣再生醫療產業正處於一個關鍵的歷史轉折點,甚至已具備了彎道超車的條件。未來生醫產業的競爭,不再只是實驗裡的研發競賽,同時也是工程師的製程競賽、資本家的資源競賽。再生醫療產業被寄予厚望成為台灣下一個三十年的產業支柱,全球生技軍備競賽已經開打,台灣要發展CDMO的黃金時刻,就是現在。
資料來源:
- 資誠(PwC Taiwan)與財團法人台灣醫界聯盟基金會「再生醫療與次世代療法產業趨勢報告」。

延伸閱讀&電子報訂閱連結:
【詳細內容請見《北美智權報》398期;歡迎加入NAIPNews網站會員成為我們的訂戶,以掌握最關鍵的專利商標智財消息!】
























