在藥品研發的長征中,開發商最恐懼的莫過於在投入數億美金後,才發現與監管機構的認知存在鴻溝。本文將專門針對美國食品藥物管理局(U.S. FDA)的正式溝通機制進行深度介紹,帶領讀者透視這套精密且高度制度化的「對話規則」。
實際上,FDA 並非單純的「審查者」,更是在科學標準上的「對話者」。對於 Regulatory Affairs (RA) 職人而言,如何透過 美國 FDA 特有的 Type A、B、C、D 各類會議,以及創新的 INTERACT 機制,將研發的不確定性降至最低,是一場關於溝通、數據與時程管理的戰略博弈。
-------------------------------------------------------------------------------------------------------
職人聲明: 本文內容係基於 FDA 現行 Guidance (如 Formal Meetings Between the FDA and Sponsors or Applicants) 之個人實務經驗彙整。內容僅供學術交流參考,不代表官方意見。
-----------------------------------------------------------------------------------------------------------------------------
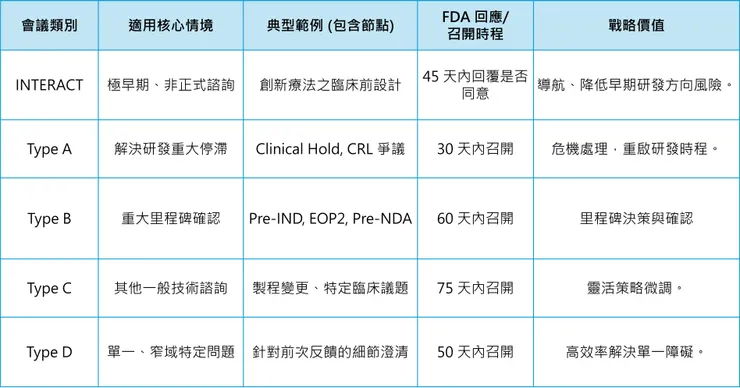
為了讓讀者快速掌握精髓,我們先透過下表綜覽這些會議的「性格」與「戰略地位」。
此外,申請者在申請時,可以提出希望 FDA 提供回覆的方式 (例如實體會議、線上會議,或是書面回覆 Written Response)。依據經驗,FDA 回覆的時間通常都蠻準時的,不會早也不會晚,不要期待可以提早拿到 FDA 的回應 (笑)。但 FDA 是否接受此申請,以及採取的回覆方式,就由 FDA 自行決定了。即使廠商想要和 FDA 召開線上會議,但目前的情況是,除非有特殊的議題,不然 FDA 通常只會提供書面回覆,畢竟和廠商開會也是壓力挺大的。
一、 研發初期的導航儀:INTERACT 會議
在正式進入 IND 之前,對於許多創新療法(如細胞治療、基因治療或複雜生技產品),廠商常面臨「無前例可循」的技術困境。這時,INTERACT (INitial Targeted Engagement for Regulatory Advice on CBER/CDER ProducTs) 會議便扮演了關鍵角色。
1. 適用情境: 當產品還處於臨床前開發(Pre-clinical)的極早期,甚至連 Pre-IND 會議都還嫌太早時,INTERACT 提供了一個非正式的諮詢管道。它主要針對藥理、毒理實驗設計或初步的 CMC(化學製造管制)定性提供建議。
2. 實務重點: INTERACT 的目的是協助廠商在進行昂貴的 GLP 實驗前,確認方向是否偏離 FDA 期望。值得注意的是,INTERACT 會議不屬於正式的 PDUFA (Prescription Drug User Fee Act,處方藥使用者付費法案) 所規範的審查時程。PDUFA 是美國一項重要的法律,允許 FDA 向藥廠收取審查規費,以換取承諾在特定的時限內完成審查任務;然而,儘管 INTERACT 不在這些法律保障的倒數時限內,它對於縮短後續正式 IND 的審查障礙,仍具有極高的導航價值。
二、 救火與里程碑:Type A 與 Type B 會議
這兩類會議是藥品開發中最核心、也最常被啟動的溝通機制。
1. Type A:處理研發停滯的「救命草」
Type A 會議(Stalled Product Development Meetings)的本質是「危機處理」。
- 適用情境: 最常見於收到 Clinical Hold(臨床暫停)通知、或是收到 CRL(完整回應函)後對補件路徑有重大爭議時。此外,若因安全性問題導致研發中斷,也屬於此類。
- 實務重點: Type A 的特點是「快」,FDA 通常在收到申請後 30 天內就會召開。這不是輕鬆的討論,而是開發商必須帶著紮實的數據與解決方案,去尋求監管機關「放行」的談判場。
2. Type B:研發生命週期的「節點確認」
Type B 是所有 RA 最耗費心力準備的里程碑會議,涵蓋了產品從雛形到上市的關鍵時刻,包括:
- Pre-IND Meetings: 確認臨床前數據足以支持進入人體試驗。
- End-of-Phase 1 (EOP1) 與 End-of-Phase 2 (EOP2): 這是研發的分水嶺。特別是 EOP2,它定調了後續關鍵試驗(Pivotal Trial)的設計。如果 FDA 對三期試驗的 Endpoints(終點指標)或樣本數有異議,而廠商未在此時達成共識,未來的上市申請失敗。
- Pre-NDA/BLA Meetings: 在正式提交上市申請前,確認數據呈現格式與查核準備。
三、 靈活諮詢與精準打擊:Type C 與 Type D 會議
1. Type C:客製化的技術對話
Type C 涵蓋了「不屬於 A、B、D 的所有其他討論」。
- 適用情境: 它是最靈活的工具,適合討論特定的技術問題。例如:製程變更、新的生物標記評估、或是針對特定亞群患者的臨床設計微調。
- 實務重點: 雖然 Type C 的排程較長(約 75 天),但它是廠商微調開發策略、降低後期風險的最佳日常工具。
2. Type D:針對單一問題的「快速特攻」
這是 FDA 在 PDUFA VII 中正式納入的新型會議,旨在提高行政效率。
- 適用情境: 專門處理「單一、窄域」的議題。如果你只需要詢問一個關於 CMC 的特定檢驗方法,或者對 FDA 之前的某個反饋有細節疑問,不需要動用大規模團隊時,Type D 是最佳選擇。但這裡要注意的是,如果 FDA 在收到申請後,認為問題的規模較大,需要較多的審查時間,會將此申請轉為 Type C 會議。
- 實務重點: 申請後 50 天內召開,FDA 參與人員更精簡,能有效避免為了小問題而卡住大進度的窘境。
四、 職人實務:會議成功的「理性格點」
與 FDA 開會,成功的關鍵不在於會議當天的口才,而在於背後的戰略佈局:
- 問題的封閉性: 千萬不要問「FDA 您覺得這設計好嗎?」這種開放式問題。正確的問法應是:「基於附件 A 的數據,我們認為採用指標 X 是合理的,FDA 是否同意?」這能逼使監管機構給出明確的科學反饋。
- Meeting Package 的品質: 這是溝通的靈魂。一份優良的 Meeting Package,應該要能提供 FDA 審查員清楚的提問,以及充足的支持性資料,讓審查員能夠藉由這些資料,提供精準地回覆。如果審查員回覆的是「您提供的資料不足,我們無法提供明確的回覆」,那就白白浪費了許多的時間。
- 會議紀錄的法律地位: 會議結束後,FDA 發出的 Meeting Minutes 是具有準法律效力的。RA 必須精準解讀紀錄中的每一個「建議」,因為那往往是未來查核時的依據。
【結語:從「對話」到「對位」】
在醫藥法規的理性構圖中,每一場 FDA 會議都是一次「對位」的過程,能讓廠商的研發速度,與監管機構的標準對齊。精明的開發商不會將其視為法規負擔,而是將其視為產品增值的機會。透過對 Type A-D 以及 INTERACT 的精準選擇,我們才能在充滿變數的法規環境中,走出一條最短且最穩健的通關路徑。
參考資料:
Formal Meetings Between the FDA and Sponsors or Applicants of PDUFA Products Guidance for Industry



















