什麼是內毒素? 為何在無菌製劑中很重要?
內毒素 (Endotoxin) 為組成革蘭氏陰性菌外膜脂多醣 (lipopolysaccharide; LPS) 複合體一部分。當細菌死亡或用人工方法破壞後,細菌外膜裂解將會釋出脂多醣片段,在宿主內啟動內毒素的致毒機制。內毒素不是蛋白質,因此十分耐熱而且穩定,在100℃的高溫下加熱1小時也不會被破壞,故在一般濕熱滅菌的標準下 (121℃, 12 min) 也無法將其破壞,只有在160℃的溫度下加熱2到4個小時,或使用強鹼、強酸或強氧化劑加溫煮沸30分鍾才能破壞它的生物活性。
細菌內毒素廣泛存在於自然界中,如自來水中含內毒素的量為1至100 EU/ml。當內毒素通過消化道進入人體時並不產生危害,但內毒素通過注射等方式進入血液時則可能引起熱原反應 (被定義為任何可能導致發燒的物質)、微迴圈障礙、內毒素休克或播散性血管內凝血等。因此,生物製品類、注射用藥劑、化學藥品類、放射性藥物、抗生素類、疫苗類、透析液等製劑以及醫療器材類(如一次性注射器,植入性生物材料)必須經過細菌內毒素檢測試驗合格後才能使用。因為上述原因故內毒素的限量以及允收標準的設定就很重要了,以作為產品放行至市場上的最後關卡。
如何制訂藥品規格有關細菌內毒素限量之允收標準?
依據中華藥典第八版之 (7008) 細菌內毒素檢驗法,內毒素限量 (endotoxin limit) 計算公式為K/M。其中,K為可產生發熱反應之內毒素閾值 (threshold) 劑量,以每 Kg 體重單位劑量(IU/Kg) 表示;M為藥品每 Kg 體重之最大建議使用劑量。當藥品須在固定時間內多次注射或連續輸注時,M為1小時內之最大總投給劑量。各藥品之內毒素限量單位可定義為IU/mL、IU/mg等。(原文:https://www3.cde.org.tw/faq/faq_more?id=1022)
關於內毒素 Endotoxin 詳細公式應該是寫在 USP <1085> Guidelines on the endotoxins test。
Endotoxin limit = K/M
K = 5 EU/kg for most routes of administration or 0.2 EU/kg for intrathecally administered drugs (不同給藥途徑會有不同的K值!!! 詳見 table 2)
M = maximum recommended dose of product per kilogram of body weight of the patient or maximum total dose administered in a 1-hour period (與給藥劑量相關,詳見 table 2))
K及M都是每單位體重,因此帶入哪個體重不影響;如果是持續輸注或是一日多次給藥,M會以每小時最大給藥量估計。
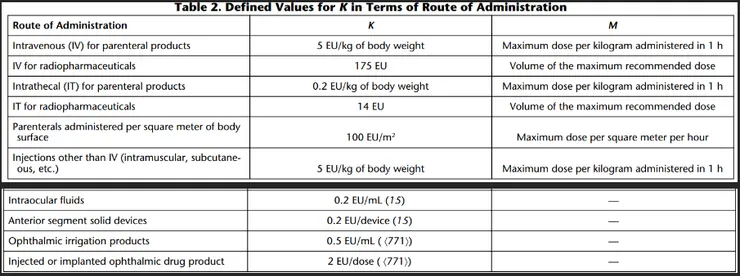
USP <1085> Table 2























