缺血性中風治療出現新曙光!亞家生技與國衛院、輔大生命科學系攜手合作研究計畫,透過動物試驗模擬人類的病理過程,最新結果發現,源自於人類臍帶間質幹細胞(WJ-MSCs)的外泌體(Exosomes),透過靜脈注射至中風大鼠體內,能顯著改善活動功能、促進神經修復,詳細成果12月發表於國際再生醫學期刊《Cell Transplantation》,可望為外泌體治療應用,開闢新的可能性。
圖說:國內最新研究發現,源自人類臍帶間質幹細胞的外泌體,對於缺血性中風的大鼠,能顯著改善活動功能並促進神經修復。(資料來源:亞家生技)
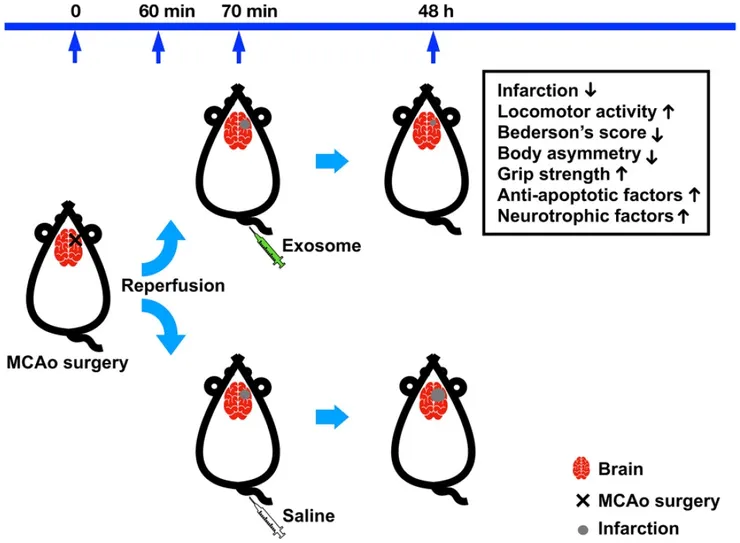
為了進一步了解外泌體對缺血性中風的治療效果,研究團隊將老鼠右側大腦中動脈血管阻塞一小時後再輸通,分為試驗與對照兩組,各別注射外泌體和生理食鹽水,於兩天後進行一系列測驗,包括神經功能缺損評估、身體不對稱性、抓握力與活動能力測試等,比較中風後的恢復情況。結果顯示,注射外泌體後的中風大鼠,在抓握力測試中,力量顯著提升,從中風初期的200至300克,進步到400克左右,恢復至一般老鼠66%的水準。而水平移動時間、站立次數也都明顯改善,相較未接受治療組別,行動更加靈活,平衡感亦獲提升。
研究團隊透過組織切片分析更發現,大鼠在注射外泌體後,跟對照組相比,腦梗塞體積明顯縮小,腦組織損傷狀況也減少。國衛院合聘副研究員、輔大生命科學系副教授陳雲翔指出,外泌體展現了對腦部微環境的調控能力,「缺血的腦組織中,抗細胞凋亡因子(如Bcl-2、Bcl-xL)及神經滋養因子(如BMP7、GDNF)的表達均有增加,這些對神經細胞的存活和功能修復至關重要」,不只促進神經組織修復,還能調節發炎反應,證實外泌體在缺血性中風的早期治療應用中頗具潛力。

圖說:亞家生技透過產學合作提供設備等技術資源,該研究採用「製藥用無菌隔離裝置」進行細胞與外泌體培養等操作,有效降低環境與人為汙染的可能性。(資料來源:亞家生技)
另外,研究將大鼠腦部皮質的神經元細胞進行體外實驗,利用麩胺酸(glutamate)刺激造成損傷,再與外泌體共同培養,觀察受損狀況是否改善。結果發現穩固微血管結構的重要蛋白MAP2表達增加,染色體斷裂減少,代表細胞存活狀況更好,並減少細胞凋亡。研究團隊認為,這表示外泌體具有保護神經細胞的功能,可顯著對抗麩胺酸造成的毒性損害,加上外泌體內含許多生物活性分子,包括多種微型核糖核酸(microRNA)、細胞激素與生長因子,仍需進一步探討作用機制,釐清外泌體抵達受損腦組織的途徑,並評估不同劑量和治療時間,以及確認長期治療效果,將有助於腦中風患者。

圖說:醫啓健康診所院長林孝祖於12月醫科展中,分享外泌體於醫美領域的實際應用經驗。(資料來源:亞家生技)
目前外泌體在醫美領域,主要集中於促進皮膚修復和抗衰老。醫啓健康診所院長林孝祖於12月醫科展講座中指出,不像細胞治療可能引發免疫排斥,「外泌體優勢在於分子小、吸收快、安全性高,尤其可穿越血腦屏障,對於腦中風病患具有重要意義。」因為中風後的復健期相當漫長,如果外泌體能有效促進神經修復,將有助於患者縮短復健時間,提升生活品質,未來還可應用在阿茲海默症、帕金森氏症等其他神經退化疾病,可望帶來新的治療選擇。
◎研究論文網址:























