一套把「早知道不行」變成制度的決策方法
製藥產業裡,最昂貴的失敗,從來不是臨床三期做出陰性結果本身,而是你其實在更早之前,就已經有機會知道它不該走到那一步。
這也是輝瑞過去十多年最值得反覆研究的地方。根據輝瑞 2022 年發表於 Drug Discovery Today 的總結,到 2020 年底,該公司從 first-in-human 到核准的端到端臨床成功率,已從 2010 年的 2% 提升到 21%,高於當時約 11% 的同業平均;而 2016 到 2020 年間獲批產品中,有 75% 至少拿到一項 expedited regulatory designation。這不是單純靠運氣變好,而是背後的研發決策邏輯真的被重寫了。如果把這場轉型濃縮成一句話,它的核心並不是「更敢押注創新」,而是更早用定量方法證明:這顆藥到底有沒有真的在人體裡,按照你以為的方式發揮作用。而輝瑞把這套思路制度化後,形成了業界最常被提到的框架之一:3 Pillars,後來又進一步落到 SOCA(Signs of Clinical Activity) 這套早期決策體系。
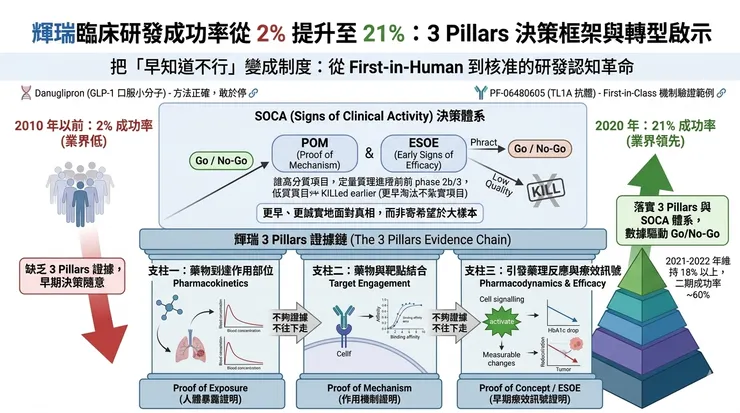
一、3 Pillars 並不是管理口號,而是從失敗案例裡倒推回來的「最低真相標準」
3 Pillars 的誕生,並不是因為有人在會議室裡發明了一個漂亮口號,而是因為輝瑞在 2000 年代中後期回頭檢視自家失敗管線時,發現很多案子其實死得很晚,卻不是因為問題很晚才出現,而是因為早期根本沒有把最基本的事情問清楚。
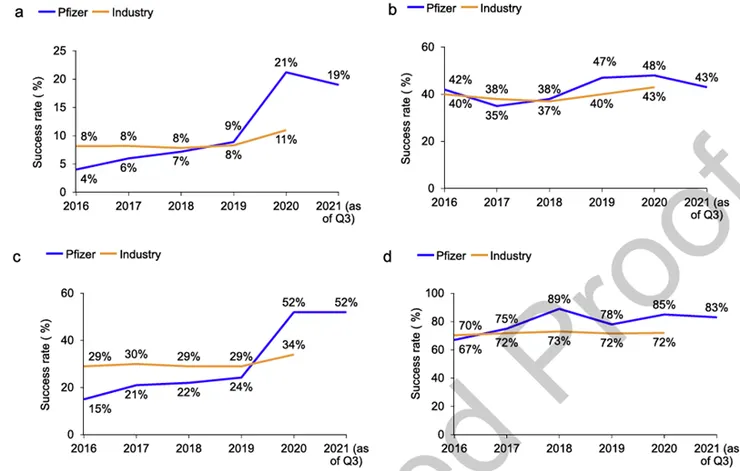
圖1:2016年至2021年第三季度,輝瑞與行業整體的首次人體試驗至獲批成功率對比。(a)首次人體試驗至獲批的累計成功率。(b) I期新分子實體(NMEs)成功率。(c) II期新分子實體(NMEs)成功率。(d) III期及批准階段新分子實體(NMEs)的累計成功率。
具體來說,很多候選藥物在一開始證明了安全性,甚至看到一些零碎的 biomarker 變化,就被推進到更昂貴、更大型的後期試驗;但到了真正驗證療效時,團隊才意識到:原來藥物並沒有穩定進到作用部位,或根本沒有有效結合目標靶點,又或者雖然結合了,卻沒有轉化成足夠的藥理反應。等到這些真相在二期、三期才浮現,成本已經高得嚇人。輝瑞後來的結論很清楚:要降低 attrition,不是靠更樂觀,而是要更早建立一套「不夠證據就不要往下走」的制度。
也因此,3 Pillars 其實只回答三個看似簡單、卻極難被真正做扎實的問題。
- 第一,藥物能不能到達作用部位。這是 pharmacokinetics 的問題。藥物如果到不了該去的組織、細胞或受體周邊,再漂亮的體外親和力都沒有意義。
- 第二,藥物到達後,能不能真的與目標藥理靶點結合。這不只是 in vitro binding assay,而是要在人體內建立 target engagement 的證據。
- 第三,結合之後,能不能在作用部位引發與療效相關的藥理反應。這就是 pharmacodynamics,也是真正把「分子作用」往「臨床可能有效」推進的關鍵一跳。
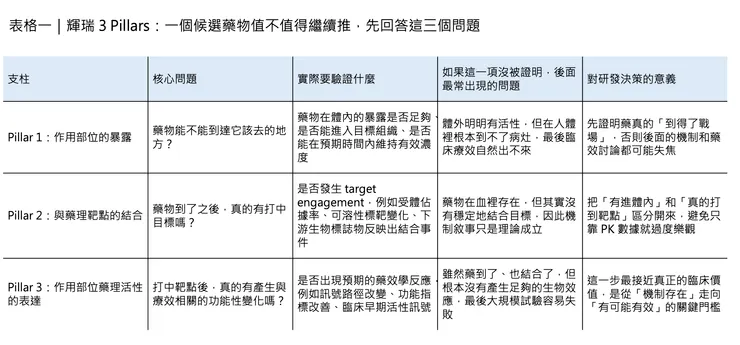
如果把這三個支柱翻成更直白的語言,其實就是:
你先得證明這顆藥到了戰場;接著證明它真的打中敵人;最後還得證明打中之後,不只是冒個煙,而是真的造成了你預期的效果。這三件事缺一不可。因為在輝瑞的框架裡,真正危險的不是失敗,而是在沒有這三層證據鏈的情況下,還自以為已經足夠接近成功。
二、從 3 Pillars 到 SOCA:輝瑞真正厲害的,不是提出原則,而是把原則變成「卡關機制」
很多公司其實也知道早期應該更重視 Proof of Mechanism,但真正難的是,怎麼把這種共識變成日常研發決策,而不是每次都在壓力下破例。
輝瑞後來往前走了一步,把 3 Pillars 進一步制度化為 SOCA(Signs of Clinical Activity) 框架。根據輝瑞自己的回顧,SOCA 的精神是讓每個早期專案在進入關鍵研究前,就先定義好:你到底要用什麼數據、什麼 target value、什麼時間點,來證明它值得下一輪投資。換句話說,SOCA 不是做完試驗再來「看看有沒有亮點」,而是在試驗開始前就先約定,什麼才算通關。
在這套框架裡,兩個概念特別重要。
- 一個是 POM(Proof of Mechanism),也就是證明藥物在人體內真的打到了它該打的機制。
- 另一個是 ESOE(Early Signs of Efficacy),也就是在較早期階段先看到足以支持後續投資的早期療效訊號。
前者更偏向「你真的有作用到該作用的地方嗎」,後者則更像「這種作用,開始在病人身上產生我們想要的方向了嗎」。兩者合起來,形成輝瑞在早期 go / no-go 決策裡最重要的硬門檻。
這件事聽起來像流程管理,但本質上其實是一場文化改革。因為它要求團隊從「把研究做大、把資料做多」的慣性,轉向「設計一個最關鍵的 killer experiment,盡快回答最值錢的未知問題」。而這種改變之所以有效,正是因為它把研發裡最容易被拖延、最容易被情緒化處理的 kill decision,往前拉到了成本還相對可控的階段。
三、Danuglipron:一個很好的「加速決策」案例,也是一個很好的提醒——方法正確,不代表分子一定成功
如果要找一個最能說明 3 Pillars / SOCA 如何幫助專案加速推進的例子,danuglipron(PF-06882961) 很有代表性。
Danuglipron 是一款口服小分子 GLP-1 receptor agonist。對這類專案來說,最有利的地方在於:GLP-1 這條機制並不是完全未知的黑盒子。從 liraglutide 到 semaglutide,整個產業早就知道活化 GLP-1 receptor 能帶來降糖與減重效果。也就是說,對輝瑞而言,真正的未知不在「這個機制有沒有生物學合理性」,而在「這顆口服小分子能不能在人體內,重現這條機制的臨床價值」。這種情況下,團隊就可以把 3 Pillars 的重心放得更實際:不必重新發明整個生物學,而是更快去驗證人體內暴露、可接受安全性,以及早期糖代謝 readout。
後來公開的臨床資料確實證明,danuglipron 在第二型糖尿病與肥胖研究中,都能帶來有統計意義的 HbA1c、fasting plasma glucose 與體重下降。2023 年 JAMA Network Open 的二期資料顯示,在 T2D 患者中,部分 BID 劑量相較 placebo 的 HbA1c 降幅可達超過 1%;2025 年發表的 obesity phase 2b 研究也顯示,它能帶來具臨床意義的體重下降。從早期臨床訊號角度看,這其實是一個典型 ESOE 被快速讀出的案子。
但 danuglipron 之所以更有教育意義,不只因為它展示了早期加速決策的價值,還因為它提醒了另一件事:**一套好的決策框架,可以提高整體成功率,卻不能保證每顆分子最後都會走到上市。**2025 年 4 月,輝瑞最終宣布終止 danuglipron 開發,原因是一位受試者出現可能的 drug-induced liver injury,雖然停藥後已恢復,但公司在綜合現有臨床資料與監管意見後,認為風險效益比不再支持繼續推進。
這個結果並不削弱 3 Pillars 的價值,反而更證明它的本質:它不是保證成功的魔法,而是一種更早、更誠實面對真相的方法。
Danuglipron 的故事說明,哪怕專案一度有很好的 ESOE,只要後續安全性或可競爭性出了問題,仍然應該停止。對一家大型藥廠來說,這種「即使可惜,也敢停」的紀律,本身就是研發效率的一部分。
四、PF-06480605:當機制是新的,3 Pillars 真正的價值就更清楚了
相較於 danuglipron 這種建立在已驗證機制上的項目,PF-06480605 更能展現 3 Pillars 在 first-in-class 專案裡的真正意義。
這是一款針對 TL1A(TNF-like ligand 1A) 的單株抗體。今天大家對 TL1A 在 inflammatory bowel disease 的價值已經比較熟悉,但在 PF-06480605 早期開發時,這仍屬於高不確定性的全新路線。也正因如此,團隊若要往後走,最重要的就不是「先做大試驗看看」,而是先在健康受試者與病人中,一步一步把支柱一、二、三補齊。(PMC)
2019 年發表的 first-in-human phase 1 研究顯示,PF-06480605 在健康受試者中整體耐受性良好,且暴露隨劑量大致上升;更重要的是,研究者透過 serum total soluble TL1A 的劑量依賴性增加,證明了 target engagement。這一點非常關鍵,因為它不是只說「藥有進到血裡」,而是更進一步證明:藥到了、也抓住了它該抓的靶點。
接下來的問題就變成:這種 target engagement,能不能轉譯成真正和疾病改善相關的藥理效果?而這正是第三支柱最難、但也最值錢的部分。之後的 ulcerative colitis 研究顯示,PF-06480605 在中重度 UC 患者中,確實觀察到臨床、內視鏡與組織學層面的改善訊號。這類資料的重要性不在於它已經證明最終商業成功,而在於它幫助團隊逐步把「TL1A 是個有趣靶點」推進到「TL1A 在人體內可能真的具有可轉譯的治療價值」。
這種案子和 danuglipron 剛好形成對照:
danuglipron 所處的是「機制已被外部世界證明,分子本身要快速過關」;PF-06480605 則是「分子與機制都需要逐步建立可信度」。而 3 Pillars 的高明之處,就是它能同時服務這兩種完全不同的專案,只是關注重點不同。
五、輝瑞真正改變的,不只是成功率,而是研發決策的時間點
從結果回看,這場轉型最值得記住的,不只是「21% 對 2%」這個漂亮數字,而是它背後所代表的決策前移。
輝瑞 2022 年的總結寫得很清楚:這波 turnaround 的關鍵驅動之一,就是 enhanced data-driven decision making;而公司 2023 年年報也進一步指出,到 2022 年底,輝瑞從 first-in-human 到核准的成功率維持在 18%,同時到 2021 年底 NME 的 phase 2 success rate 達到 60%,高於產業中位數 37%。這些數字說明,3 Pillars / SOCA 並不是一時有效的管理運動,而是確實在一段時間內重塑了專案篩選品質。
更重要的是,這種提高效率並不是靠只做低風險項目換來的。輝瑞自己在回顧中強調,2016 到 2020 年獲批產品中有 75% 至少拿到一項 expedited designation,這說明它提升成功率的同時,並沒有把創新性一起削平。真正的重點在於:不是少做創新,而是更早把不夠紮實的創新淘汰掉,把資本和時間留給真正有機會過關的項目。
六、寫在最後:3 Pillars 的真正啟示,不是「更會做試驗」,而是更早面對真相
輝瑞這個案例之所以值得被反覆討論,不只是因為它把成功率做高了,而是因為它提供了一種很不一樣的研發態度。
在藥物開發裡,我們很容易把「繼續推進」誤認為一種正向行為,把「終止專案」看成失敗;但從組合管理的角度看,真正危險的,往往不是停掉一個案子,而是明明還沒有證明它真的打中了機制、真的能在人體內產生有意義的藥理效應,卻因為 sunk cost、內部期待或外部壓力,硬把它送進下一輪更昂貴的試驗。
3 Pillars 最深層的價值,恰恰在這裡。

它要求團隊在早期就誠實地回答:藥到了嗎?打中了嗎?打中之後真的有用嗎?
如果三個問題裡有一個還答不出來,那麼真正負責任的做法,不是把希望寄託在更大的樣本數或更長的時間上,而是先停下來,把最值錢的未知問題釐清。這不只是對資本市場負責,更是對病人和科學本身負責。
所以,輝瑞把臨床成功率從 2% 拉到 21%,表面上看像是流程優化,骨子裡卻是一場認知革命:
研發成功,不是因為你更會說服自己往前走,而是因為你更有能力在早期就看穿哪些專案不該走下去。
------
參考資料:
[0]: 各公司官網&公開資料
[1]: https://www.sciencedirect.com/science/article/pii/S1359644621005444 "Achieving end-to-end success in the clinic: Pfizer’s learnings on R&D productivity - ScienceDirect"
[2]: https://www.sciencedirect.com/science/article/pii/S1359644620304360
[3]: https://pubmed.ncbi.nlm.nih.gov/34127852/ "Danuglipron (PF-06882961) in type 2 diabetes: a randomized, placebo-controlled, multiple ascending-dose phase 1 trial - PubMed"
[4]: https://jamanetwork.com/journals/jamanetworkopen/fullarticle/2805054
[5]: https://www.pfizer.com/news/press-release/press-release-detail/pfizer-provides-update-oral-glp-1-receptor-agonist
[6]: https://pmc.ncbi.nlm.nih.gov/articles/PMC7098865/ "First‐in‐human, randomized dose‐escalation study of the safety, tolerability, pharmacokinetics, pharmacodynamics and immunogenicity of PF‐06480605 in healthy subjects - PMC"
[7]: https://pubmed.ncbi.nlm.nih.gov/34126262/
[8]: Fernando, Kathy,et al."Achieving end-to-end success in the clinic: Pfizer’s learnings on R&D productivity." Drug discovery today (2021).














