
圖片作者:ChatGPT
最近看《生物學學理解碼2》的時候,看到一段話讓我忍不住挑眉。書裡寫道:
「豆漿或牛奶加入酸之後,pH值下降至等電點時可引發蛋白質凝聚沉澱。」這句話聽起來很有學問沒錯,可是我一看到就覺得不對勁——如果鹹豆漿的製作真的得精準調整 pH 到等電點,那早餐店老闆根本沒辦法做生意了!
如果真要調等電點,鹹豆漿怎麼可能這麼快端上桌?
我們先簡單科普一下:大豆蛋白的等電點(isoelectric point)大約在 pH 4.5~5.0。在這個酸鹼值下,蛋白質表面電荷為零,不再互相排斥,容易聚集形成沉澱。這是製作豆腐、豆花等豆製品時常見的原理。做豆花與豆腐時,製作者會小心控制凝固劑(像是石膏、鹽滷、檸檬酸)的量,讓豆漿的pH值慢慢降,這樣大豆蛋白就可以緩緩凝結,形成滑順的豆花。
但鹹豆漿不是這樣做的。
你在早餐店看到的鹹豆漿流程,是這樣的:
- 醋、醬油、鹽巴、榨菜等調味料先放進碗底
- 豆漿煮滾,燙燙地倒進去
- 幾秒鐘內出現像豆花一樣的凝塊,香氣四溢
這個過程沒有任何人拿出 pH 試紙,也沒有人在做「一滴一滴地微調酸鹼值」這種工夫。要真這樣搞,一碗鹹豆漿起碼要做 10 分鐘,老闆生意怎麼做?
真相:聽過「衝擊式凝固」(shock coagulation)沒有?
鹹豆漿凝固的關鍵,在於食品科學中所謂的「衝擊式凝固」。這種凝固方式,與其說是精準控制,不如說是瞬間打亂。
當我們把熱豆漿倒入含有醋的碗中時,局部的酸性上升使豆漿中的蛋白質在瞬間發生變性。這些蛋白質本來在中性 pH 下能夠穩定懸浮,但遇到酸的「突襲」,電荷平衡被破壞,蛋白質互相吸附、聚集、形成絮狀凝塊。這不是均勻整鍋一起沉澱,而是局部變性的結果。
這不是什麼「準確控制」,而是「環境劇變」。
鹹豆漿不是豆花,也不是豆腐
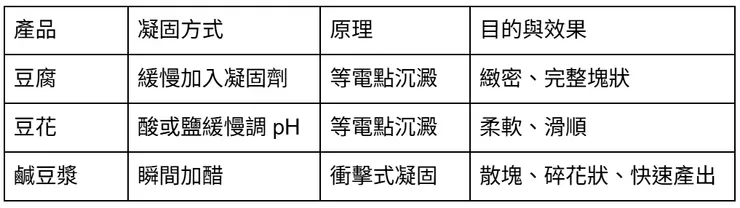
所以,同樣都是「大豆蛋白凝固」,但機制與目的不同。
作者:老葉
鹹豆漿凝結的條件其實很簡單,只需要加酸(可能還有一點鹽)。不需要精密儀器,單純只靠生活經驗。這也是為什麼它能成為小吃攤、早餐店的日常供應品,而不是食品工廠專屬。
我們不是在否定等電點的科學概念,而是提醒:不要為了硬套理論而忽略現場實情。許多食品科學的現象,在實務上呈現的形式並不如課本那樣教條。
鹹豆漿的成功,是一場突如其來、無需計算的凝結,不是 pH 滴定的實驗成果。這或許正是它讓人喜愛的地方:簡單、快速、帶點混亂美感,卻好吃極了。
最後補充一點關於蛋白質的小知識:不只是酸會讓蛋白質凝固變性,鹼也會;另外溫度、鹽濃度改變,也都會讓蛋白質凝固變性。

圖片作者:ChatGPT
豆漿在加熱時,蛋白質會經歷熱變性(thermal denaturation)。這代表原本摺疊好的蛋白質開始打開,露出疏水性區域,使它們更容易彼此吸附。這也是為什麼你不能用冰豆漿來做鹹豆漿,因為不夠熱的話,蛋白質不會變性、也不會凝結。
鹽分,特別是食鹽(氯化鈉 NaCl),能影響水中離子強度,改變蛋白質表面的電荷屏蔽效果,進一步促進蛋白質的聚集與沉澱。鹹豆漿裡的醬油、榨菜、鹽巴其實都在貢獻這個效果。這種情形在食品科學中有個名詞叫「鹽析」(salting-out),在某些蛋白質中效果特別明顯。
在鹹豆漿裡,主要是醋的加入快速改變了豆漿的pH值,使蛋白質電荷重新分布,再加上熱與鹽的共同作用,最終導致蛋白質變性沉澱。
這三個條件同時發生,就好比三面包抄,讓豆漿中的蛋白質措手不及、紛紛投降結團。
然後熱呼呼的鹹豆漿就上桌啦!

























