2025 年對全球生物製藥產業來說,並不是輕鬆的一年:利潤壓力持續、資本市場保守、監管門檻趨嚴,許多公司被迫收縮管線、集中火力。但在這樣的環境下,真正有臨床說服力的創新項目反而更顯得「拉開距離」。
一端,是已經進入成熟階段的技術——例如 GLP-1 相關代謝藥物,開始走向第二、第三波疊代;另一端,則是過去 10~30 年都被視為「研發黑洞」的領域,首次出現具有結構性意義的數據:亨廷頓氏舞蹈症(Huntington’s disease)、阿茲海默症(Alzheimer’s disease)等。以下整理 2025 年最具代表性的五個臨床里程碑,從科學、臨床與商業三個角度看它們可能重塑哪些版圖。

01 uniQure 亨廷頓氏舞蹈症基因療法:延緩疾病進展 75%,打開 30 年無藥可治的缺口
亨廷頓氏舞蹈症(Huntington’s disease, HD)是一種體染色體顯性遺傳的致命神經退化疾病,由 HTT 基因第 1 外顯子 CAG 重複序列異常擴增所導致。突變的 huntingtin 蛋白(mHTT)在神經元中逐步累積,引起運動障礙、認知功能下降與精神症狀,大部分患者在 30–50 歲起病,病程往往長達 10–25 年,最終多因吞嚥困難導致吸入性肺炎、感染或心衰竭而死亡。
目前臨床上核准的僅有 tetrabenazine 與其升級版本 deutetrabenazine 這類 VMAT2 抑制劑,只能緩解舞蹈樣不自主運動,對疾病根本進程沒有改變。
近十多年被寄予厚望的,是直接針對 mHTT 的「致病機制導向」療法,包括:
- antisense oligonucleotide(ASO):Roche / Ionis 的 tominersen 就是一例,但其 III 期試驗 GENERATION HD1 在 2025 年 3 月正式宣告終止,主要因為在臨床效益與安全性上未達預期;
- 寡核苷酸編輯與 siRNA / PNA 技術:例如 Wave Life Sciences 的 WVE-003(PNASO),2024 年公布的 I 期多劑量數據顯示,24 週與 28 週時腦脊髓液中 mHTT 降幅約為 46% 與 44%,算是早期但有意義的訊號。
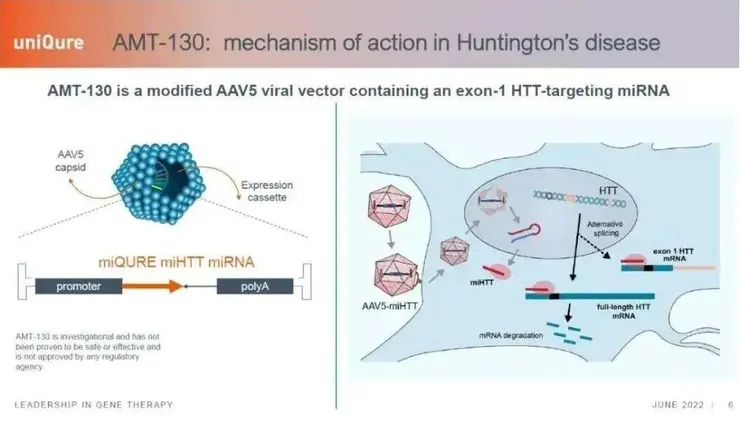
真正把整個領域的期待往前推一大步的,是 uniQure 的基因療法 AMT-130。
2025 年 9 月 24 日,uniQure 公布了 AAV5 載體遞送 micro-RNA 的基因療法 AMT-130,在早期 HD 患者 1/II 期試驗的長期追蹤結果。
這項研究最關鍵的幾個點是:
- 高劑量組疾病進展減緩約 75%:相較於自然病程預期,疾病進展率被大幅拉慢,且效果可持續至少 3 年;
- 成果與先前 2 年隨訪觀察到約 80% 疾病進展減緩相當,顯示療效具備穩定性;
- 在衡量患者生活自理能力的 Total Functional Capacity(TFC) 指標上,與對照組相比,疾病惡化速度約減緩 60%;
- 其他臨床量表(運動、認知等)亦呈現一致的正向趨勢;
- 安全性輪廓整體可控,未見新的嚴重毒性訊號。
從機制角度來看,AMT-130 建立在 uniQure 專利的 miQURE 基因沉默技術 上:
- 利用 AAV5 作為載體,將人工設計、可辨識 HTT mRNA 的 micro-RNA 序列直接送入腦部;
- 讓神經元在體內「長期表達」這段 micro-RNA,持續抑制 mHTT 的產生;
- 目標是一次給藥、長期降低毒性蛋白累積,從源頭改變疾病進展。
在監管路徑上,uniQure 先前的計畫是 2026 年提出 BLA 申請,希望以 1/II 期長期追蹤資料作為關鍵證據。然而,面對近年 FDA 對基因療法態度轉趨保守,公司在 2025 年再次對外說明:
目前的 1/II 期數據「不太可能單獨作為 BLA 的主要證據」,因此 uniQure 正重新檢視試驗設計,並預計在 2026 年第一季與 FDA 進行後續會議,討論是否需要額外的 confirmatory study 或更大樣本數據。
即便如此,AMT-130 已經是 HD 領域迄今最有說服力的疾病修飾(disease-modifying)候選療法。
真正的難題,已經從「科學可不可行」,轉向:
- 單次治療定價與健保/保險給付模式如何設計;
- AAV 生產、神經外科給藥與長期隨訪的醫療系統承載能力;
- 以及在基因療法安全事件頻仍後,監管單位對風險—效益比的再平衡。
對投資人與產業來說,這不只是 uniQure 一家公司的故事,而是整個神經退化性基因療法能否真正跨過「從漂亮生物標記到實際臨床獲益」這道關鍵門檻的試金石。
02 Metsera GLP-1 減重新星:月打一次、部分數據超過 tirzepatide,引爆百億美元併購戰
肥胖與代謝症候群是 GLP-1 之戰的主戰場,但 2025 年真正吸睛的一幕,來自一家成立不久的公司——Metsera。
2024 年 9 月,Metsera 首次公開其長效 GLP-1 皮下注射劑 MET-097i 的早期數據:
在一項短短 36 天的研究中,受試者平均體重已減輕 7.5%,這在 GLP-1 競品中即使作為「開胃菜」也相當驚人,於是迅速被納入全球肥胖藥物投資雷達。
Metsera 採用的科學切入點在於「biased agonism(偏向型活化)」:
- 傳統 GLP-1 receptor agonists 同時活化 G-protein 與 β-arrestin 路徑;
- β-arrestin 雖然參與受體內吞與訊號調控,但也與受體脫敏、部分不良反應相關;
- MET-097i 被設計成選擇性偏向 G-protein 訊號,希望在維持甚至放大減重與降糖效果的同時,減少因過度 β-arrestin 活化造成的耐受性問題與腸胃道副作用。
在給藥頻率上,MET-097i 也走出差異化路線:
當 Novo Nordisk 的 Wegovy(semaglutide) 與 Eli Lilly 的 Zepbound / Mounjaro(tirzepatide) 都屬於 每週注射一次 時代,Metsera 直接瞄準 「每月注射一次」 的長效設計,對慢性體重管理的依從性非常具有吸引力。
2025 年 1 月公布的 I 期試驗 細節進一步撐高了市場預期:
- 研究納入 120 位超重或肥胖、但尚未罹患第二型糖尿病的受試者;
- 每週注射 12 週後,MET-097i 組的平均體重減輕 11.3%(相對於安慰劑校正);
- 在 12 mg 劑量組中,個別受試者的體重下降幅度可達 約 20%,尚未觀察到明顯平台期。
9 月下旬,Metsera 又釋出一項 IIb 期試驗 結果:
- 在 1.2 mg 劑量組中,至第 28 週時,安慰劑校正後平均體重減輕為 14.1%;
- 研究延長到 36 週時的探索性分析顯示,體重仍持續下降,尚未見到明確 plateau;
- 部分個體的最大體重降幅高達 26.5%。
有分析師直接拿這個數據與 tirzepatide 比較:在類似追蹤期間,tirzepatide 的安慰劑校正體重減輕約為 13%,這讓 MET-097i 的競爭力從「有潛力的後來者」,變成「可能改寫劇本的選手」。
Metsera 的第二支王牌,則是超長效 amylin 類似物 MET-233i。Amylin(胰淀素)本身就參與飽足感、胃排空與葡萄糖調控,被視為 GLP-1 的天然「搭檔」。
在 2025 年 6 月公布的一項 I 期試驗裡:
- MET-233i 在 36 天內,與安慰劑相比,平均體重減輕 8.4%;
- 個別受試者的降幅更達 10.2% 左右;
- 公司已明確表示,後續戰略重點之一,就是 MET-097i 與 MET-233i 的聯合療法,試圖在不劇烈增加不良反應的前提下,達成更深、更持久的體重控制。
在這樣的數據與故事下,併購戰很快開打。
- 9 月中,Pfizer 先出手,以企業價值 49 億美元(每股 47.50 美元現金)收購 Metsera,再加上最高 24 億美元 里程碑金,總對價可達 73 億美元;
對連續終止兩個口服 GLP-1 候選藥 lotiglipron 與 danuglipron 的 Pfizer 來說,這筆交易幾乎是「重返肥胖戰場」的關鍵賭注。 - 一個月後,Novo Nordisk 半路殺出,以企業價值 60 億美元(每股 56.50 美元)與最高 90 億美元 的潛在總價碼加入競標。
Metsera 對這個條件表現出明確興趣,讓戰局急轉直下。
Pfizer 隨即反擊:
- 一方面提高報價,最終將企業價值拉高至 70 億美元(每股 65.60 美元),並提出最高 每股 20.65 美元 里程碑金,總交易規模逼近 100 億美元;
- 另一方面走法律戰,指控 Novo Nordisk 濫用肥胖市場既有優勢、企圖透過併購壓制競爭。
最終,Pfizer 在訴訟與出價上都取得上風,完成這筆接近百億美元的交易。

對產業來說,Metsera 案例重要的不是又多了一筆「天價併購」,而是它傳遞了一個訊號:
在 GLP-1 已被視為紅海時,真正有差異化技術與明確臨床優勢的後來者,仍然可以撬動巨頭做出非常激進的資本決策。
03 Novo Nordisk Amycretin:GLP-1 / Amylin 雙重作用,為「後 semaglutide 時代」搶先布局
雖然在 Metsera 競購戰中失手,Novo Nordisk 並非手上沒有牌。2025 年,它用一組相當漂亮的 II 期數據,證明自己在「下一代減重降糖藥物」上仍握有主導權——主角就是 Amycretin。Amycretin 是 Novo Nordisk 自研的 長效 GLP-1 / amylin 受體雙重激動劑:
- GLP-1 負責促進胰島素分泌、抑制胃排空、增加飽足感;
- Amylin 則在抑制進食、延緩胃排空與調節葡萄糖動力學中扮演關鍵角色;
- 透過同時活化兩者,理論上可在 體重控制與血糖管理 上取得比單一 GLP-1 更深的效果,且不必完全依賴不斷提高 GLP-1 劑量。
在 2025 年年初公布的 I/IIa 期肥胖試驗 中:
- 對沒有糖尿病的超重/肥胖受試者,使用每日口服 20 mg Amycretin 治療 36 週;
- 平均體重降幅約 22%,對照組則約 2%,差距極為明顯。
更具指標性的,是後續針對第二型糖尿病患者的 II 期試驗:
- 研究納入 448 名使用 metformin、是否合併 SGLT2 抑制劑皆可的 2 型糖尿病患者;
- 比較 每週一次皮下注射 與 每日一次口服 Amycretin 的療效與安全性;
- 在第 36 週時:
- 皮下注射高劑量組體重平均降幅 14.5%(對照安慰劑 2.6%);
- 口服高劑量組體重平均降幅 10.1%(對照安慰劑 2.5%);
- 兩種給藥途徑在 36 週都尚未出現明顯體重 plateau,代表後續延伸治療仍可能帶來額外減重。
- HbA1c 降幅方面:
- 皮下注射組最高降幅約 1.8 個百分點;
- 口服組最高降幅約 1.5 個百分點。
在 GLP-1 競賽當中,這組數據被視為 Novo Nordisk 的「信心回復劑」。過去一年,Novo Nordisk 雖然憑藉 Wegovy(semaglutide) 率先打開減重市場,但:
- Wegovy 的市佔逐步受到 Eli Lilly Zepbound(tirzepatide) 侵蝕;
- 公司寄望極高的 GLP-1 / GIP 雙重激動劑 CagriSema,在 2024 年的 REDEFINE-1 試驗中雖有 22.7% 體重減輕 的亮眼數字,卻仍低於市場對「下一代明星藥」的預期,引發市值單日蒸發約 720 億美元 的劇烈反應;
- 在神經退化領域,semaglutide 於 EVOKE 與 EVOKE+ 研究中未能顯著延緩阿茲海默症的進展,雖然本就被視為高風險探索,但結果公布後股價仍回落約 10%。
在這樣的背景下,Amycretin 的成功顯得格外關鍵——它代表 Novo Nordisk 不再只是在 GLP-1 單一維度提升劑量,而是開始用「多重激動」重新定義代謝治療結構。
接下來的節奏已經排好:
- 公司計畫於 2026 年第一季 啟動皮下注射與口服 Amycretin 用於超重與肥胖成年人的 III 期全球試驗;
- 之後還將推進多個多重標靶共激動劑,包括 GLP-1 / GIP / glucagon 三重激動劑(部分由亞洲合作夥伴 The United Laboratories 引進),以及兩款靶向 GLP-1 / GIP / amylin 的三標靶候選藥物。
在國際間,Amgen、Eli Lilly、AstraZeneca 等也都佈局了自家三重激動劑與多標靶代謝藥物,未來幾年,「GLP-1 是減肥藥」這個直觀印象,很可能被一整個 multi-agonist 世代所替代,Amycretin 肯定會是其中重要的一支。

04 BMS / BioNTech PD-1 / VEGF 雙抗:全球數據對齊,中美日多地同步推進雙標靶抗體戰局
在腫瘤免疫治療領域,「PD-1 / VEGF 雙重封鎖」這個概念並不陌生。Roche 的 atezolizumab + bevacizumab 組合已在肝細胞癌(HCC)等多個適應症拿到標準治療地位,證明 免疫檢查點封鎖 + 抗血管生成 的協同具備臨床實力。接下來的自然演化,就是把兩種機制壓縮成 一支雙特異性抗體(bispecific antibody),在劑量控制與藥代 / 分布上獲得更大主導權。
這條路線在中國首先由 Akeso / Summit Therapeutics 的 ivonescimab(PD-1 / VEGF 雙抗) 打出名號:
在晚期非小細胞肺癌(NSCLC)的頭對頭試驗中,ivonescimab 在無進展生存期(PFS)上壓過 Keytruda(pembrolizumab),引起全球關注。
2025 年,這個故事在另一組主角身上走向全球化——BioNTech 與 Bristol Myers Squibb(BMS) 的 pumitamig(BNT327)。

pumitamig 的結構設計相當精緻:
- 由一個人源化 anti–PD-L1 單域抗體(VHH) 與一個含 Fc-silencing 突變的 anti-VEGF-A IgG1 抗體 融合而成;
- 一端與 PD-L1 結合,恢復效應 T 細胞的活化與腫瘤免疫監視;
- 另一端中和 VEGF-A,改善腫瘤微環境中的免疫抑制與異常血管生成;
- 透過「一支抗體,雙重機制」,在藥動學與暴露控制上有機會優於傳統兩藥聯合。
BioNTech 最初透過與中國 biotech Pumis 的策略合作獲得這個資產,隨後在 2024 年直接以約 9.5 億美元 收購 Pumis,將 BNT327 全數納入自家管線。這筆收購也被視為 BioNTech 從 mRNA 疫苗轉向「多平台腫瘤公司」的重要一步。2025 年 6 月,BMS 宣布以高達 111 億美元 的對價,取得 pumitamig 的全球共同開發與商業化權利——在當下生技併購市場裡,這個量級已屬頂規。
臨床數據方面,pumitamig 先是在中國完成多項早期試驗,接著走向全球化。
9 月公布的一項 全球 II 期試驗,針對 廣泛期小細胞肺癌(extensive-stage SCLC, ES-SCLC):
- pumitamig 聯合標準化療,在未接受過先前治療的 ES-SCLC 患者中,取得 76.3% 的確認客觀緩解率(cORR);
- 疾病控制率(DCR)達 100%;
- 整體結果與 2025 年歐洲肺癌大會(ELCC)上公布的中國拓展隊列數據高度一致,等於完成了「跨地區、跨族群療效一致性」的第一輪驗證。
本月針對 晚期三陰性乳癌(triple-negative breast cancer, TNBC) 的全球 II 期數據亦已對外發表:
- 無論腫瘤 PD-L1 表達高低,pumitamig + 化療都展現出有臨床意義的活性;
- 確認客觀緩解率 cORR 為 61.5%,疾病控制率 DCR 達 92.3%;
- 再次印證先前在中國進行之 TNBC Ib/II 期試驗的趨勢,而這次是以更國際化的患者結構與多國中心完成。
在開發策略上,BioNTech 與 BMS 已將 pumitamig 推進至同一適應症的後期階段,啟動 III 期 ROSETTA-LUNG-01 試驗,目標是進一步檢驗其在 NSCLC 一線治療中的長期獲益與安全性:
- 試驗跨越美國、英國、土耳其、中國、韓國、澳洲等多國,未來還會持續擴點;
- 預計在 2029 年 3 月完成 主要數據收集。
同時,歐美日多家藥廠也在布局 PD-(L)1 / VEGF 雙標靶或類似組合:
部分採取 雙抗體連用(如 PD-1 + VEGF 抑制劑),部分則研發自有的 bispecific 抗體平台(如部分歐洲與日本公司在固體腫瘤上的 PD-L1 / VEGF 或 PD-1 / CTLA-4 / VEGF 三標靶設計)。
pumitamig 的意義,不只是一支雙抗多賺幾個適應症,而是:
用全球一致的臨床數據,證明「免疫檢查點 + 抗血管生成」不只是 combo,也可以是高效率、高控制度的雙特異性平台。
這對後續所有想做 PD-1 / VEGF 或其他雙標靶抗體的公司來說,都是一個非常具體的 benchmark。
05 Roche 阿茲海默症 Brainshuttle 計畫:從 gantenerumab 失敗,到 trontinemab 帶來深度 Aβ 清除的可能
阿茲海默症(Alzheimer’s disease, AD)長期被視為「研發黑洞」:過去 20 多年裡,數百個候選藥物在不同機制上折戟,其中相當一部分瞄準 β-amyloid(Aβ)。
近幾年,lecanemab 與 donanemab 等抗 Aβ 抗體終於在早期 AD 患者中展現出減緩認知退化的能力,給整個領域打了一劑強心針,但在療效深度、安全性(尤其是 ARIA-E / ARIA-H)與給付問題上,爭議仍然很大。
Roche 在這場戰役中,其實曾站在失敗者的一方。
2022 年底,Roche 的 Aβ 抗體 gantenerumab 在兩項大型 III 期試驗中皆未能達到主要終點,整個專案被迫按下停止鍵。但 Roche 並沒有就此放棄,而是把焦點轉向一個關鍵問題:
也許不是抗體本身完全失敗,而是「進入大腦的劑量與方式」出了問題。
這就引出了他們的創新藥物遞送技術 Brainshuttle,以及 2025 年備受關注的候選藥物 trontinemab。
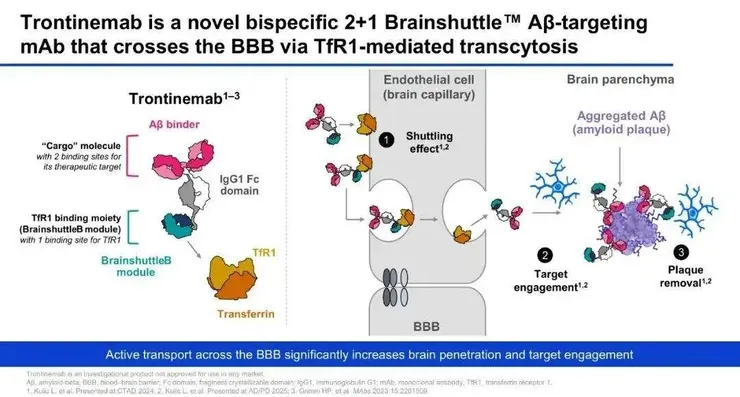
簡化來說,Brainshuttle 的設計邏輯是:
- 選擇一個在血腦屏障(BBB)上高度表達的受體 —— Roche 選的是 transferrin receptor 1(TfR1);
- 將針對病理目標的抗體(這裡就是 gantenerumab)與一個可結合 TfR1 的蛋白域融合成單一分子;
- 抗體一端抓住 TfR1,被腦血管內皮細胞「誤認為營養物質」,透過 receptor-mediated transcytosis 運送到腦實質;
- 一旦跨過 BBB,抗體便能在中樞真正接觸到大量 Aβ 斑塊,透過 antibody-dependent cellular phagocytosis(ADCP) 促進小膠質細胞清除;
- 因為大腦暴露提高,可以用 更低的系統性劑量 達到相似甚至更強的中樞效果,有機會減少全身及腦內不良事件。
Trontinemab 正是 gantenerumab 與 TfR1 結合域「2+1」的產物。
Roche 自 2023 年在阿茲海默症臨床試驗會議(CTAD)首次公開 trontinemab 的 I 期爬坡數據後,就持續被業界關注。真正引發熱議的,是 2025 年在阿茲海默症協會國際會議(AAIC)上公布的 Ib/IIa Brainshuttle AD 試驗 結果:
- 在接受 3.6 mg/kg 高劑量 trontinemab 並治療約 7 個月的患者中,
- 91% 在 PET 掃描中達到「澱粉樣蛋白陰性」標準,
- 其中 72% 達成所謂 「deep clearance(深度清除)」,即大腦 Aβ 負荷降至非常低的水平;
- 與現有抗 Aβ 抗體相比,初步觀察到的 ARIA 發生率與嚴重度都有下降趨勢,顯示在更低全身暴露下,中樞清除效果反而更好;
- 在 2025 年 CTAD 上,Roche 再次重申:
- 低劑量、低給藥頻率即可達到強力 Aβ 清除,
- 且安全性 profile 相較現有療法更具優化空間。
基於這些結果,Roche 已啟動兩項平行的 III 期 TRONTIER-1 與 TRONTIER-2 研究,鎖定早期 AD 患者族群,希望回答幾個關鍵問題:
- 深度 Aβ 清除是否能轉化為更明確、持久的認知與功能獲益?
- 在多種共病與實際臨床環境下,Brainshuttle 模式是否仍能維持安全邊際?
- 與既有抗 Aβ 抗體相比,trontinemab 的「風險—效益比」是否足以支撐差異化定價與付款方接受度?
從更宏觀的角度看,trontinemab 的價值不僅止於「Roche 終於在 AD 找回場子」,而是:
它證明了一條路:在中樞神經疾病裡,不只是「藥對不對」,還包括「能不能把藥足夠聰明地送進大腦」。
如果 Brainshuttle 在 AD 上成功,它的概念完全可以外溢到帕金森氏症、亨廷頓氏舞蹈症、ALS 甚至部分精神疾病,為整個 CNS 領域打開新的技術軌道。
結語:
臨床數據開始「分出等級」,真正的勝負已不只在實驗室裡決定回顧這五個 2025 年的關鍵進展,可以看到幾個共通特徵:
- 都是高難度適應症或高度擁擠賽道中的「質變級」數據:
- HD 基因療法從症狀緩解走向病程修飾;
- GLP-1 與多重激動劑在減重上不再只是「多幾公斤」,而是重新競逐整個代謝治療版圖;
- PD-1 / VEGF 雙抗與 Brainshuttle,則分別代表腫瘤免疫與 CNS 治療在「給藥智慧化」上的重要一步。
- 每一個故事背後,都同時牽動著幾十億甚至上百億美元的資本與交易布局:
基因療法定價模式、GLP-1 / obesity 市場併購、PD-1 / VEGF 雙抗全球授權、AD 抗體與付款方的拉鋸,都會在未來 3–5 年分別寫下第二、第三幕。 - 對 Biotech 與投資人來說,臨床「質」的差異,正快速放大「命運」的差距:
在資本愈來愈挑剔的環境下,只有像 AMT-130、MET-097i / MET-233i、Amycretin、pumitamig、trontinemab 這樣,能在臨床端說出足夠清楚、足夠有數據支持的故事,才有資格去談下一階段的商業化與管線放大。
2025 年也許不是最喧鬧的一年,但很可能是未來回頭看時,會被標記為:
「很多長期趨勢第一次被真正證明『可以跑得通』的一年。」
接下來,考驗的將不只是科學,而是誰能在監管、商業模式、定價與全球佈局上,把這些突破變成真正可持續的產業回報與患者獲益。

參考資料:
- www.biospace.com/drug/5-of-2025s-defining-clinical-wins
- 公開資料&各公司官網














