台北時間 10 月 6 日下午,萬眾矚目的 2025 年諾貝爾生理學或醫學獎出爐。諾貝爾基金會將今年的獎項授予 Mary E. Brunkow 博士、Fred Ramsdell 博士與 坂口志文(Shimon Sakaguchi) 博士,以表彰他們對「外周免疫耐受(peripheral immune tolerance)」機制的突破性貢獻——也就是免疫系統如何在戰鬥之餘,避免誤傷自身組織的核心原理。

▲ 由左至右依序為 Mary E. Brunkow、Fred Ramsdell、坂口志文 (Shimon Sakaguchi)
今年三位得主的研究答案很直接:身體內存在一群專職「踩煞車」的免疫細胞——調節性 T 細胞(regulatory T cells, Tregs)。它們會抑制過度活化的免疫反應,確保「清道夫」不會反咬主人。
諾貝爾委員會主席 Olle Kämpe 表示:「這些發現對理解免疫系統如何運作至關重要,也幫助我們解釋,為什麼不是每個人都會發展成嚴重的自體免疫疾病。」
關鍵科學脈絡:從胸腺「篩選」到外周「監督」
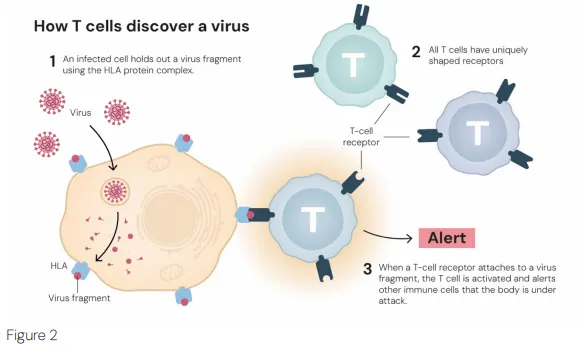
▲ 圖片揭示了 T 細胞如何發現病毒
在 1990 年代中期之前,主流觀點認為免疫耐受主要靠「中樞耐受(central tolerance)」:T 細胞在胸腺分化時,若對自身抗原反應太強會被淘汰。但 坂口志文(Shimon Sakaguchi) 在 1995 年 提出顛覆性見解:外周也有一套獨立機制,透過一群表現 CD25 等標誌的 T 細胞來抑制免疫反應;他把這群細胞定義為 調節性 T 細胞(Tregs)。這是第一個清楚指出「免疫系統不只會踩油門,也有專職踩煞車的人」的里程碑。
2001 年,Mary E. Brunkow 與 Fred Ramsdell 解析了為何某些小鼠會自發出現嚴重自體免疫疾病:罪魁禍首是 FOXP3 基因突變(著名的 scurfy 小鼠)。更關鍵的是,他們也觀察到人類若帶有 FOXP3 缺陷會罹患 IPEX syndrome(immunodysregulation–polyendocrinopathy–enteropathy, X-linked)——一種致命的自體免疫–內分泌–腸道炎症聯合症候群。
兩年後(2003 年),Sakaguchi 團隊把線索完整串起來:FOXP3 是 Tregs 的「主控開關」,沒有它,這群煞車細胞就無法正常分化與維持功能,外周免疫耐受也會崩解。至此,「胸腺篩選+外周監督」的雙層安全網才算被完整描繪。
Tregs 到底怎麼「踩煞車」?
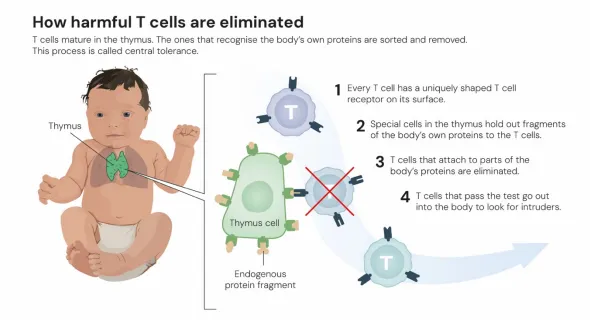
▲ 圖片揭示了有害的 T 細胞如何被消滅
為什麼一個轉錄因子 FOXP3,能讓 Tregs 這麼關鍵?因為它驅動了整套抑制程式:
- 資源競爭:Tregs 高表現 CD25(IL-2 受體 α 鏈),會「搶走」環境中的 IL-2,讓效應 T 細胞(Teff)難以持續擴增。
- 分泌抑制性細胞激素:如 IL-10、TGF-β,降低發炎迴路。
- 接觸依賴抑制:上調 CTLA-4 等分子,削弱抗原呈現細胞(APC)的活化能力。
- 代謝改寫:影響局部乳酸、色氨酸代謝環境,讓 Teff 難以維持效能。
此外,Tregs 不只一種來源:
- Thymic Tregs(tTregs):在胸腺分化完成,負責維持對「自體」的耐受。
- Peripheral Tregs(pTregs):在外周遇到特定抗原與環境訊號後轉化,常見於黏膜與發炎組織,扮演微環境「調頻器」。
這些機制共同確保免疫系統既能對外強硬、對內溫柔——「戰而不狂,攻而不傷己」。
醫療版圖的影響:從自體免疫到癌症與移植
三位得主開啟的是一整個研究與臨床轉譯的領域。今天我們看到多條策略正走向臨床:
- 自體免疫疾病:利用 低劑量 IL-2 或 工程化 IL-2 變體(IL-2 muteins),選擇性擴增 Tregs;正在探索的還有 抗原特異性 Tregs 與 CAR-Tregs,期望「只在錯誤戰場上踩煞車」。
- 器官移植:Tregs 有望降低排斥反應與免疫抑制藥物用量,改善長期移植存活與生活品質。
- 腫瘤免疫:腫瘤往往「招兵買馬」把 Tregs 拉進腫瘤微環境,抑制抗腫瘤反應;如何精準削弱腫瘤中的 Tregs、同時保留全身耐受,是後免疫檢查點時代的重要課題。
- 過敏與發炎性疾病:藉由提升黏膜 Tregs 功能,有望重設過敏閾值,減緩反覆發作。
換言之,Tregs 不是單一藥物靶點,而是一個設計治療「力道與選擇性」的大開關。這也是為何諾貝爾委員會強調其對醫學的「決定性意義」。
得獎者簡介
- Mary E. Brunkow, PhD(1961 年生)
普林斯頓大學博士。現任西雅圖 Institute for Systems Biology(系統生物學研究所)資深專案經理。2001 年以 FOXP3–scurfy 的關鍵研究寫下外周耐受的基石之一。 - Fred Ramsdell, PhD(1960 年生)
1987 年加州大學洛杉磯分校(UCLA)博士。現任舊金山 Sonoma Biotherapeutics 科學顧問,長年專注 T 細胞調控與自體免疫機制。 - 坂口志文 (Shimon Sakaguchi), MD, PhD(1951 年生)
1976/1983 年於日本京都大學獲醫學士與博士,現為 大阪大學免疫學前沿研究中心特聘教授。1995 年提出 CD25+ Tregs,2003 年將 FOXP3 定位為 Tregs 的主控轉錄因子。
把免疫的「煞車系統」從概念變成可操作的生物學與臨床工具——這就是 2025 年諾貝爾生醫獎所嘉獎的成就。它改寫我們對免疫平衡的理解,也為自體免疫、移植與腫瘤治療提出了更精準、更智慧的下一步:在對抗疾病與保護自身之間,找到那條真正最安全的線。
讓我們恭喜這三位科學家!
參考資料:
- 各公司官網&公開資料
- The Nobel Prize in Physiology or Medicine 2025. Retrieved October 6, 2025, from https://www.nobelprize.org/prizes/medicine/2025/summary/
- They understood how the immune system is kept in check. Retrieved October 6, 2025, from https://www.nobelprize.org/uploads/2025/10/popular-medicineprize2025.pdf






















